CROMATOGRAFÍA
La técnica de cromatografía de adsorción es un proceso que se realiza constantemente en los laboratorios de todo el mundo para la separación de mezclas de compuestos tanto orgánicos como inorgánicos que la mayoría de las veces solo se pueden separar por otros procedimientos muy difícilmente. Las mezclas de compuestos incoloros también se pueden separar por estos procedimientos aunque como es natural ciertos detalles deben ser modificados de acuerdo con la naturaleza de la sustancia que se ha de separar.
Hay varios factores que deben tomarse en cuenta en la elección de un adsorbente para una separación cromatografica determinada. Desde luego debe ser insoluble en el disolvente que se va a utilizar para la separación y no debe reaccionar con las sustancias que van a separarse ni debe actuar como catalizador de sus descomposición, transposición o isomerización, ha de tener un compuesto uniforme prescindiendo de su origen y debe ser incoloro cuando sean de localizar visualmente las unas correspondientes a compuestos coloreados.
Teóricamente cuando menor sea el tamaño de las partículas del adsorbente mayor será el grado de separación de la mezcla tratada sin embargo desde el punto de vista practico se debe tener en cuenta que cuanto menor sea el tamaño de las partículas menor será la velocidad con la que el disolvente o la solución pasaran atraves de la columna, por tanto se necesita una situación de compromiso. El adsorbente no debe ser ni de grano muy grueso ni muy fino, el diámetro medio de las partículas debe ser de unas 8 a 12 micras. Cuando necesariamente se tienen que utilizar como adsorbente polvo muy fino , la velocidad de la solución o el disolvnt6e atreves d el adsorbente se puede aumentar mezclando este con un coadyuvante de filtración tal como el “HYFLOSUPERCEL” la aplicación de una subsidian suave ( de unos 680mm) o de cierta precisión puede también acelerar la velocidad del disolvente atreves de la columna el adsorbente mas utilizado es la alumina (AL203) la a variedad de alumina con mayor poder de adsorción no se puede preparar calentando al rojo la alumina activada comercial durante unas cuantas horas y dejándola después de enfriar en un desecador a vacio. Sin embrago la lumina activada de esta forma es un adsorbente demasiado fuerte resultando difícil la eliminación del producto adsorbido en la columna.
Para usos generales se puede preparar un producto mas adecuado calentando la alumina comercial periodos de tiempo mas cortos a temperaturas mas bajas o bien añadiendo deliberadamente agua a las aluminas deshidratadas a temperaturas mas altas.
El poder adsorbente de un producto determinado depende no solo d esu naturaleza sino también del disolvente utilizando en la preparación del cromatograma. Por tanto no es posible establecer una clasificación rigurosa del poder adsorbente relativo a las distintas sustancias que se pueden utilizar. Sin embrago se puede establecer aproximadamente la siguiente clasificación : adsorbentes muy activos : alumina con un contenido de agua pequeña , carbón activado y arcilla ., adsorbentes intermedios: gel de sílice , acido silícico, carbonato de calcio, fosfato de cálcico, magnesia y cal apagada, adsorbentes débiles: sacarosa , inulina, almidón y talco.
En una separación determinada de una mezcla de compuestos por cromatografía se pueden emplear diferentes disolventes para llevar el soluto a la columna para desarrollar el cromatograma eluir el producto absorbido. Aunque generalmente en una separación se utiliza un solo adsorbente, existen fases en los que resulta ventajosos el empleo de 2 o mas adsorbentes simultáneamente, por lo general para llevar las mezclas de compuestos a al columna se utiliza un disolvente relativamente poco polar: para el desarrollo de cromatograma un disolvente algo po.lar , y para la elución de productos adsorbidos , un disolvente mas polar todavía. Los disolventes mas frecuentes se pueden ordenar según su polaridad creciente : éter de petróleo , tetracloruro de carbono, sicloexano, sulfuro de carbono, éter, acetona, benceno, esteres de ácidos orgánicos, cloroformo, alcoholes, agua, piridina, ácidos orgánicos y mezclas de ácidos o bases con agua, alcohol o piridina. Por ejemplo en una separación cromatografica la mezcla de compuestos se puede llevar la columna disuelta en éter de petróleo, el cromatograma se puede desarrollar con benceno y las diferentes bandas o zonas se pueden diluir con etanol.
APARATOS
En su forma más sencilla las 2 únicas piezas necesarias para la cromatografía son:
1._ La columna que es un tubo de vidrio terminado en su parte inferior en un tuvo mas estrecho en el que se pone un poco de algodón para detener el adsorbente dentro del tubo.
2._ Un quitasato la columna se puede conectar al quitasato mediante un tapón d e corcho goma taladro si el tubo de la columna es bastante mas largo que la columna o altura del adsorbente su parte superior libre puede servir como deposito del disolvente si no se pude adaptar a la parte de la columna superior un deposito adicional, que puede ser un embudo de llave.
La capacidad de adsorción de los compuestos orgánicos esta determinada es decir los compuestos que se adsorben mas fuerte son:
1.- Ácidos carboxílicos.
2.- Alcoholes, aminas y tioles.
3.- Aldehidos, cetonas y esteres.
4.- Haluros orgánicos.
5.- Hidrocarburos no saturados cuanto mayor sea su capacidad de adsorción.
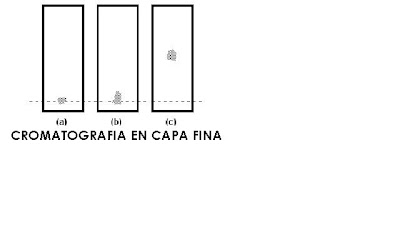
CROMATOGRAFÍAS EN FASE DE VAPOR Y EN CAPA FINA
Estos tipos de cromatografía se utilizan mucho en la identificación de compuestos orgánicos.
ADSORCIÓN CROMATOGRÁFICA
En esta operación se aprovecha la adsorción diferencial (o deposito) de los componentes de una mezcla móvil que se hace pasar sobre una fase móvil (solida, llamada adsorbente) desde 1931 la cromatografía de adsorción ha adquirido importancia para separar, concentrar, purificar y analizar sustancias. Se han descrito numerosas formas para realizarse entre ella la cromatografía de partición, en papel, en capa delgada y en fase gaseosa. Algunas de estas últimas son de mucha utilidad en estudios analíticos y en la determinación de la pureza en pequeñas cantidades (microgramos) de compuestos orgánicos.
CROMATOGRAFÍA DE SUSTANCIAS INCOLORAS
Aunque los compuestos incoloros pueden formar bandas bien definidas en una columna de adsorción cromatografica se necesita la utilización de métodos especiales para la localización de las bandas de losproductos adsorbidos y para poder separarlos convenientemente. Para la localización de las bandas de losproductos adsorbidos se emplea generalmente una lámpara ultravioleta.
Para la localización de las fracciones de una mezcla adsorbida se pueden emplear también métodos puramente empíricos por ejemplo en la columna se puede diluir con una seria de disolventes de polaridad gradualmente creciente y el filtrado (eluato) se recogen pequeñas fracciones. La eliminación de l disolvente en cada de una de estas se administrara el compuesto orgánico que ha sido eluido en ella , una ves identificado el compuesto mediante un punto de fusión o alguna otra propiedad se puede mezclar con los productos idénticos obtenidos en las fracciones próximas.
CURSO PRÁCTICO DE QIMICA ORGANICA
RAY Q BREWSTER
ALHAMBRA
1978
ESPAÑA
253 PP
QD251 B743 1970